Original: http://www.tulane.edu/~wiser/protozoology/notes/api.html
Apicomplexa ovat monophyletic ryhmä koostuu lähes kokonaan loistauti (eli ei vapaana elävät) lajeja. Apicomplexa yhdessä ripsieläimet ja panssarisiimalevät, muodostavat korkeamman asteen ryhmä tunnetaan Alveolata. Merkittävä piirre on tämän ryhmän litistetty rakkula-rakenteita sanottu aivokuoren alveolae-, joita esiintyy vain alla solukalvon. Aikaisemmin Apicomplexa olivat osa ryhmää nimeltä Sporozoa ja tämä nimi on vielä joskus käytetty. On ollut joitakin ehdotuksia palata takaisin nimen Sporozoa (Cox, Tr. Parasitol. 18: 108).
Elektronimikroskoopilla paljasti ainutlaatuisia ultrarakenteellisia ominaisuuksia joukossa eri Sporozoa jota käytettiin sitten määritellä uudelleen ryhmiin. Selvästi erottuva ominaisuus Apicomplexa on ryhmä soluelimiin löydetty toisessa päässä, jota kutsutaan kärkipään-organismin. Tämä ‘apikaalisella monimutkainen’ sisältää sekretorisen soluelimiin tunnetaan micronemes ja rhoptries, polaarinen renkaat koostuvat mikrotubulusten, ja joissakin lajeilla conoid joka sijoittuu napa soi. Jossain vaiheessa niiden elinkaaren aikana, jäsenet Apicomplexa joko hyökätä tai liittää isäntäsoluihin. Se on tänä invasiivisia (ja/tai liikkuvia) vaiheessa, että nämä apikaalisella soluelimiin ilmaistaan sekä subpellicular kalvot, jotka ovat itse asiassa aivokuoren keuhkorakkuloihin. Apikaalisella soluelimiin rooli vuorovaikutuksessa loisen isäntäsolun kanssa ja sitä seuraava hyökkäys isäntäsolun. (Katso yksityiskohtainen keskustelu isäntäsolun hyökkäystä malaria loinen.) Liikkuvien muotojen ja Apicomplexa ryömiä pitkin alustaan ei-ameboid tavalla tunnetaan luiston liikkuvuutta. Monet Apicomplexan lajit on flagelloitu- sukusoluja.
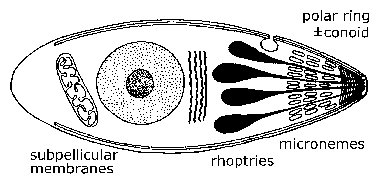
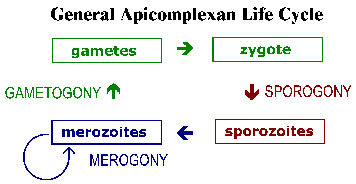
Yleinen Apicomplexan Rakenne ja Life Cycle. Invasiivisia ja/tai liikkuvia muotoja Apicomplexa näytteille erottuva hienorakenteen ominaisuudet, jotka voidaan havaita elektronimikroskoopilla. Aivan kärkipään on rengas mikrotubulusten tunnetaan napa rengas. Joskus yksityiskohtaisen cytoskeletal rakenne tunnetaan conoid nähdään myös. Pieni eliptical rakkulat tunnetaan micronemes nähdään myös tässä päässä sekä pisaran muotoinen organelles kutsutaan rhoptries.
Apicomplexa on monimutkainen elinkaari, joille on tunnusomaista kolme erillistä prosessia: sporogonia, merogony ja gametogony (kuvio). Vaikka useimmat Apicomplexa osoittavat tätä yleistä yleinen elinkaari yksityiskohdat voivat vaihdella lajin. Lisäksi terminologia, jota käytetään kuvaamaan näitä elinkaaren eri vaiheissa vaihtelee lajien välillä. Elinkaaren koostuu sekä asexually toistamaan muodot ja seksuaalisen vaiheissa. In monoxenous lajien kaikki kolme nämä prosessit suoritetaan yhdessä ainoassa isännässä ja usein yhdessä solutyypissä tai kudoksessa. Katsoo, heteroxenous lajien eri prosesseissa tehdään eri isännät yleensä syntyy eri kudoksissa.
Sporogonia tapahtuu välittömästi sen jälkeen, seksuaalisen vaiheen ja koostuu suvuton lisääntyminen, joka kulminoituu tuotanto sporotsoiittien. Sporotsoiitit ovat invasiivisia muoto, joka tunkeutuu soluihin ja kehittyä muotoja, jotka käyvät läpi toisen suvuton replikaation tunnetaan merogony. Merogony ja tuloksena merotsoiitit tunnetaan monilla eri nimillä riippuen lajista. Toisin kuin sporogonia, jossa on yleensä vain yksi kierros replikaation, usein on useita kierroksia merogony. Toisin sanoen, merotsoiitit, jotka ovat myös invasiivisia, voi reinvade soluja ja aloittaa toisen kierroksen merogony. Joskus nämä moninkertaiset merogony liittyy kytkimen isäntäorganismissa tai kytkin solutyypistä tunkeutuu loinen johtaa eri vaiheissa merogony. Vaihtoehtona suvuton replikaation merotsoiittien voi kehittyä sukusolujen prosessin kautta kutsutaan vaihtelevasti gametogony, gamogony tai gametogeneesiin. Muuntyyppisistä sukupuolisen lisääntymisen, sukusolut fuusioituvat muodostaen tsygootti, joka tehdään sporogonia.
Apicomplexa ovat erittäin suuri ja monimuotoinen ryhmä (> 5000 nimeltään lajeja). Seitsemän lajia tarttua ihmiseen (Box). Plasmodium, sillä taudin aiheuttaja malarian, on suurin vaikutus ihmisten terveyteen. Babesia on suhteellisen harvinainen zoonoottisia infektio. Muut viisi lajia ovat kaikki luokiteltu kokkidien. Kuitenkin viime aikoina molekyylitason tiedot osoittavat, että Cryptosporidium on läheistä sukua gregarines kuin kokkidilaji. Kokkidilaji pidetään yleensä opportunistipatogeeneja ja niihin liittyy usein AIDS. Useat Apicomplexan loiset ovat tärkeitä myös eläinlääketieteen ja maatalouden. Merkittävimpiä ovat Babesia ja Teileria naudoilla ja Eimeria siipikarjassa.
Levien Synty Apicomplexa |
Historiallisesti Apicomplexa on kuvattu ryhmä, jossa on vain loistaudit muotoja. Tämä ja niiden ainutlaatuinen apikaalisella soluelimiin esille kysymyksiä suhteessa siihen johtuu ryhmän. Fylogeneettinen analyysi osoittaa, että jäsenet tai sukuun Copodella muodostavat sisar ryhmä, jolla on Apicomplexa (1). Colpodellids saalistushintoja siimaleviä joka syö yksisoluisista levistä kutsutulla menetelmällä myzocytosis. Myzocytosis käsittää saalistaja (tai loinen) kiinnittämiseksi saalista (tai isäntä) ja kirjaimellisesti imevät sytoplasmassa saaliin solun kautta erikoistuneita rakenteita. Tämä kiinnitys ja vuorovaikutus saalis solu välittyy soluelimiin samanlaisia kuin että Apicomplexa käyttää kiinnittymistä varten tai invaasion isäntäsoluissa. Siten kehitystä Apicomplexa todennäköisesti kehittynyt tämän myzocytoic saalistussuunnitelmasta myzocytoic loisinta, kuten näytteillä gregarines ja Cryptosporidium, solunsisäisen parasitismin.Muut myzocytoic organismien Apicomplexa kuin apikaalisella soluelimiin kuuluvat Perkinsus, loisia ostereita ja simpukoita, ja Parvilucifera, saalistaja panssarisiimalevien. Näiden perkinsids, kuitenkin, muodostavat sisar ryhmä, jolla on panssarisiimalevät eikä Apicomplexa (kuvio). Tämä viittaa siihen, että kantaisä Panssarisiimaeliötoksiinimyrkytyksen ja Apicomplexan-alatyypit voivat ollut saalistushinnoittelua siimalevä ja että apikaalisen soluelimiin oli säilytetty Apicomplexan haaran, mutta hävisi useimmissa panssarilevää haaran.
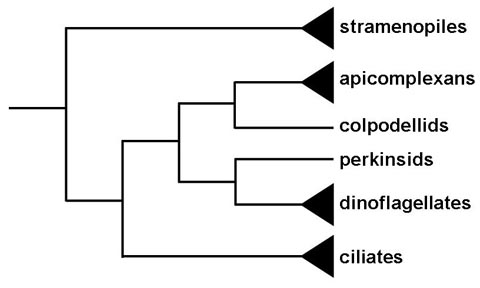 Muut välinen yhteys levät ja Apicomplexa on viherhiukkasen jäännös, jota kutsutaan apicoplast, useimmissa apicomplexans (2). Apicoplast todennäköisesti seurausta toissijaisen endosymbiosis punainen levä ja todennäköisesti sama endosymbiotic johtaneisiin tapahtumiin plastideihin panssarisiimalevien. Apicoplast on nonphotosynthetic mutta näytteille toiminta liittyy tyypin II rasvahappobiosynteesiin, isoprenoidi biosynteesiä, ja mahdollisesti hemisynteesissä. Näitä reittejä ovat olennaisesti prokaryoottisia ja ovat erinomaisia lääkekohteiden. Fotosynteettinen Alveolata, Chromera Velia, joka näyttää olevan pian haaroitus Apicomplexan on myös tunnistettu (3).
|
Kokkidien
Kokkidilaji on tunnusomaista paksuseinäisen ookystavaiheesta, joka on tyypillisesti erittyy ulosteeseen. Joissakin kokkidien (Cryptosporidium, Cyclospora, Isospora) suorittavat niiden koko elinkaaren ajan sisällä suolen epiteelisolujen vastaanottavan ja lähettävät ulosteen-suun kautta. Muut kokkidien (Sarcocystis, Toxoplasma) on monimutkaisempi elinkaaren liittyy kudoksen kystat ja useita isäntiä (eli heteroxenous).
Cryptosporidium
Koska sen Ensitunnistamisen 1907 useita Cryptosporidium-lajeja on tunnistettu erilaisia eläinten vaihtelevat kala ihmisiin. Ensimmäisen ihmisen tapauksissa kryptosporidoosia raportoitiin vuonna 1976 ja ne karakterisoitiin ripulitaudin liittyy immunosuppressioon. Aluksi uskottiin olevan harvinainen ja eksoottisen taudin. 1980- Cryptosporidium kirjattiin merkittävä syy ripulin AIDS-potilaiden ja usein johtivat kuolemaan. Kuitenkin nyt on tunnustettu, että Cryptosporidium on yleinen syy ripulia immunokompetenteilla henkilöitä ja on todennäköisesti ollut ihmisen taudinaiheuttaja alusta lähtien ihmiskunnan. Kaksi lajia tartuttamaan ihmisellä on tunnistettu: C. parvum ja C. hominis.
ELINKAARI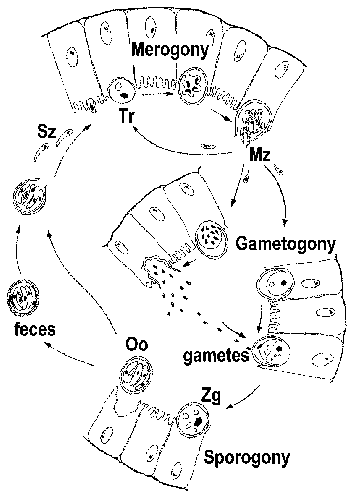
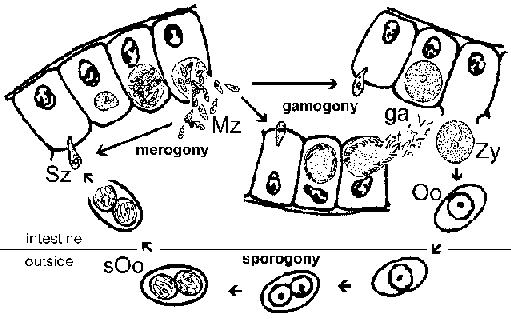
Cryptosporidium on usein luokitellaan kokkidi ja osoittaa elinkaari kuin muita suoliston kokkidien. Kuitenkin Cryptosporidium on läheisempää sukua kuin gregarines ja tämä heijastuu joitakin elinkaarensa. Infektio on hankittu nauttimisen kautta sporuloineella ookystoja (kuvio). [Katso suurempia luku elinkaaren yksityiskohtaiset legenda.] PH liittyvät muutokset kulku suolen läpi ja sapen ja haiman nesteitä ohutsuolessa laukaista excystation. Sporotsoiitteja (Sz) ilmenevät ookystien ja pitävät suolen epiteelisolujen. Toisin kuin muut kokkideja, Cryptosporidium sporotsoiiteista eivät hyökätä enterosyytteihin. Sen sijaan ne indusoivat fuusio ja laajentaminen mikrovillusten jolloin loinen tulossa ympäröi kaksoismembraani isäntä alkuperää. Liitos, nimeltään ‘syöttölaite organelle’ tai ‘liimavyöhyke’, välille muodostuu loinen ja isäntä suoliston. Loinen, kutsutaan nyt trofotsoiittivaihe (Tr), todennäköisesti johtuu ravinteiden isäntäsolun kautta tähän risteykseen. (Katsaus aiheesta ‘hyökkäys’ prosessi katso Borowski et al 2008).
Trophozoites tehdään suvuton replikaation (eli merogony) ja tuottaa 4-8 merotsoiitteihin (Mz), joka vapautuu suolen onteloon. Me- rotsoiitit tartuttaa uusi suolen epiteelisolujen ja lisäkohottaa kierrosta merogony. Lisääntynyt vakavuus taudin immuunivajepotilailla johtuu osittain niiden kyvyttömyys rajoittaa näitä ylimääräisiä kierroksia merogony.
Vaihtoehtona merogony, me-rotsoiitit voi kehittyä joko makro- tai microgametocytes infektion jälkeen, joka suoliston. Microgametogenesis liittyy useita replikaatiokierroksia vapautusta seuraa lukuisia microgametes suolen onteloon. Microgametes lannoittaa macrogametes vielä kiinni suolen epiteelisolujen. Tuloksena tsygootti (ZG) läpi sporogonia ja sporuloineella ookystien (Oo) erittyvät ulosteen mukana. Autoinfection on myös mahdollista ja tämäkin voi osaltaan lisätä sairauden vaikeusasteen immuunivajepotilailla.
VOIMANSIIRTO JA MOLEKYYLIEPIDEMIOLOGISET
Riskitekijöitä lähetyksen varten Cryptosporidiumin ovat samankaltaisia kuin muut ulosteen suun sairauksia. Kuitenkin vesiohenteiset kryptosporidioosia tautitapauksia on ollut erityisen merkittävä. Pahamaineisin on puhjennut Milwaukee keväällä 1993, jossa arviolta 400000 ihmiset kehitetty oireenmukaista kryptosporidioosi (MacKenzie et ai, New Eng. J. Med. 331: 161, 1994). Tekijöitä, jotka edistävät lisääntyneiden riskien Cryptosporidium vesivälitteinen epidemia ovat:
- pieni koko ookystien
- monenlaisia isäntäspesifisyys ja monoxenous kehitys
- tiivis yhdistysten ihmisen ja eläimen isännät
- suuri määrä ookystien erittyy (jopa 100 miljardia euroa vasikka)
- alhainen infektoiva annos
- vankka ookystien jotka ovat resistenttejä kloori
- tarttuva sporuloineella ookystien erittyy
Vaikka vaikuttavuutta noin vesi-puhkeamisen, ihmisestä ihmiseen vaikuttaa hallitsevan. Esimerkiksi oireettoman tartunnan saaneet lapset ovat yleisiä, toissijaisia tapauksia kotitalouksien korkea, ja esiintyy tavallisesti sairaaloissa, laitokset ja päiväkotien-tilanteissa tyypillisiä ulosteen-suullisella välityksellä. Molecular tutkimukset ovat paljastaneet kaksi ensisijaista genotyyppiä eristetty ihmisistä. Genotyyppi 1 on vain eristetty ihmisen lähteistä ja on ei-infektoiva hiiriä ja vasikoita. Genotyypin 2 on eristetty sekä eläinten (naudan ja lampaan) ja ihmisen lähteistä ja on tartunnan hiirille ja vasikoita. Perustuen näihin ja muihin biologisiin eroja on ehdotettu nimetä genotyyppi 1 kuten Cryptosporidium hominis (Morgan-Ryan et ai, J. Euk. Microbiol. 49: 433, 2002). Muut lajit ja genotyyppien Cryptosporidium (esim., C. felis, koira-kuin genotyyppi, jne) on eristetty AIDS-potilaista ja harvoin immuunikompetenteilta ihmisillä (Morgan et ai, J. Clin. Microbiol. 38: 1180, 2000). Kolmas laji Intian niemimaalta, C. viatorum , on myös ehdotettu (Elwin et ai, Int. J. Parasitol. 42: 675, 2012).
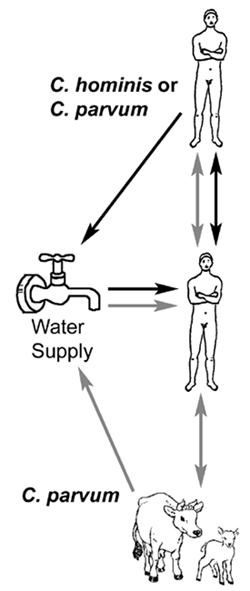
Geneettiset tiedot viittaavat siihen, että on olemassa kaksi erillistä lähetyksen lopun ihmisissä, joissa kaksi eri populaatioissa Cryptosporidiumin: 1) yksinomaan anthroponotic (eli ihmisen-to-ihmisen) syklin aiheuttama genotyypin 1 (tai C. hominis) ja 2) zoonoottista sykli aiheuttama genotyypin 2 (tai C. parvum). Zoonoottista sykli koituisi lähetyksen eläimistä (esim naudoille tai lampaille) ihmisille ja sitten myöhemmin ihmisestä ihmiseen ja mahdollisesti ihmisestä eläimen siirto. Molemmat genotyypit on osoitettu olevan etiologinen vuonna waterbourne puhkeamisen. Vesivälitteinen epidemia liittyy C. hominis johtuvat todennäköisesti veden saastumisen ihmisen viemäröinti, kun taas vesi- puhkeamisen liittyy C. parvum (genotyyppi 2) johtuvat todennäköisesti veden saastumisen lehmä tai lammas ulostetta.
SYNNYSSÄ
Yleisin kliininen ilmenemismuoto kryptosporidoosia on lievä tai Vedensekaista ripulia. Tämä ripuli on yleensä itsestään ja jatkuu useita päiviä jopa kuukauden. Recrudescences ovat yleisiä. Vatsan kouristukset, anoreksia, pahoinvointi, laihtuminen ja oksentelu ovat muita ilmenemismuotoja, jotka voivat esiintyä akuutin vaiheen. Tauti voi olla paljon ankarampi henkilöiden aids joka ilmenee kroonisena ripuli kestää kuukausia tai jopa vuosia. Jotkin AIDS potilailla on fulminantti koleran kaltainen sairaus, joka vaatii laskimoon rehydraatiohoitoa. Kuolleisuus voi olla melko korkea näissä fulminantti tapauksissa.
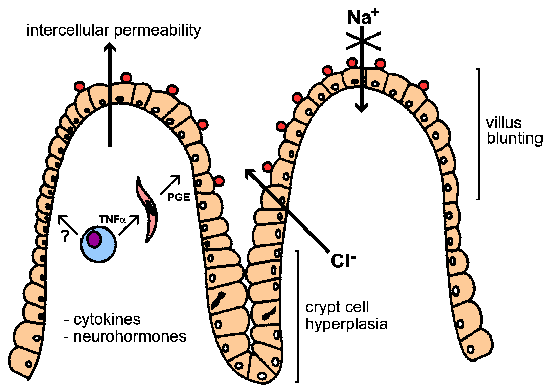
Ripuli voi olla osmoottinen, tulehduksellinen tai sekretorinen komponentit (kehikko). Vetistä luonne liittyvää ripulia Cryptosporidium infektioita on ehdottanut läsnäollessa enterotoksiinin. Kuitenkaan ole näyttöä toksiinivälitteisiä vetistä ripulia ja ponnisteluista huolimatta tunnistaa tällaiset toksiini. Kokeellinen näyttö ei viittaa siihen, että glukoosi-kytketyn Na+ imeytyminen vähenee ja Cl– eritystä kasvaa. Siksi ripuli liittyy Cryptosporidium näyttää olevan pääasiallisesti osmoottisen luonteeltaan (katso kuva). Tähän liittyy häiriöitä suolisolujen (eli suolen epiteelisolujen) -toiminto on tasaantumista Villi ja kryptassa soluhyperplasiaa. Mahdollinen mekanismi synnyssä on, että infektio suolen epiteelisolujen kanssa Cryptosporidium vahingot enterosyytteihin ja lopulta johtaa heidän kuolemaansa. Tämä laukaisee solunjakautumisen crypt alueella (eli liikakasvu) korvata vaurioituneita soluja. Yhdistelmä tuhoaminen absorboiva solujen kärjissä Villi ja kasvu CI– -secreting krypta johtaa yleisen tehostetun eritystä.
|
|
Lisäksi lisääntynyt solujen välinen läpäisevyys ja tulehduksen limakalvonalaisen kerros (alias, lamina propria) on liitetty Cryptosporidium infektio. Näiden ilmiö voisi myös edistää erittymisprosessia kautta sytokiinien ja neurohormone. Esimerkiksi, makrofagit erittävät tuumorinekroositekijä-alfa (TNF-α) tai muiden sytokiinien voi stimuloida fibroblastit ja muut solut, lamina propria erittämään prostaglandiineja (PGE) ja muita tuotteita (esim., Reaktiivisen hapen välituotteita). Kyseisiä tuotteita voidaan siten edistää eritystä ja heikentää imeytymistä.
Loinen osoittaa trofismin varten tyhjäsuolen ja sykkyräsuolen immunokompetenteissa henkilöä, kun taas infektio on laajalle levinnyt AIDS-potilailla ja ne voivat sisältää vatsa, pohjukaissuoli, paksusuolen ja sappiteiden. Tämä laajempi anatominen alue AIDS-potilailla on oletettavasti johtuu siitä, ettei immuunijärjestelmän valvoa ja rajoittaa infektiota. Soluvälitteisen immuniteetin näyttää olevan tärkeä osa immuunivasteen eliminoimaan infektion osoituksena korrelaatio alemman CD4 + T-solujen ja riski ja vakavuutta kryptosporidoosia. Interferoni-gamma, interleukiini-12, ja tuumorinekroositekijä-alfa osallistuvat suojaa Cryptosporidium -infektiota.
LISÄVIITTAUKSIA
- Clark DP, Sears CL (1996) patogeneesi kryptosporidoosia. Parasitologia Tänään 12: 221
- Guerrant RL (1997) Kryptosporidioosi: syntymässä, erittäin tarttuva uhka. Emerging. Inf. Dis. 03:51
- Greg Hannahs, Cryptosporidium: nouseva taudinaiheuttaja. http://biology.kenyon.edu/slonc/bio38/hannahs/crypto.htm
- NE Ramirez, LA Ward ja S Sreevatsan (2004) Katsaus biologian ja epidemiologian kryptosporidoosia ihmisillä ja eläimillä. Mikrobit ja Infektio 6, 773-785.
- Rose JB, Huffman DE, Gennaccaro A (2002) Riskin ja valvonta vesiliikenteen kryptosporidoosia. FEMSMicrobiol. Ilm 26: 113.
- Sunnotel, O ym (2006) Cryptosporidium. Kirjaimet Applied Microbiology 43, 7-16.
- Xiao L ja Ryan UM (2004) Kryptosporidioosi: Päivityksen molekyyliepidemiologian. Nykyinen ratkaisuehdotus Infectious Disease 17, 483-490.
- Xiao L. ja Feng, Y. (2008) Zoonoottiset kryptosporidioosia. FEMS Immunology & Medical Microbiology 52: 309-323.
Isospora
Isospora Belli uskotaan olevan pätevä laji, joka infektoi vain ihmisiä. Se on maailmanlaajuinen jakelu, mutta on yleisempää trooppisilla alueilla ja alueilla, joilla on huono sanitaatio. Infektiot ovat usein oireettomia ja niille, joiden oireet ovat yleensä itsestään rajoittava ovat kestoltaan muutaman viikon. Infektiot ovat yleisempiä ja oireet vaikeampia AIDS-potilaiden että immunokompetenteille henkilöt.
Elinkaari. Infektio on hankittu nauttimisen kautta sporuloineella ookystoja (soo). Sporotsoiitteja (SZ) ovat vapautuminen suolistossa ja tunkeutua suolen epiteelisolujen. Sisällä epiteelisolut loisen läpikäy kierroksen merogony johtaen merotsoiittisukupolven (Mz). Vapautuneet merotsoiitit reinvade suolen epiteelisolujen ja voi läpikäydä lisäkierroksia merogony tai kehittää joko mikro-tai macrogamonts. Microgametes (ga) on hedelmöittää macrogametes (ga) muodostamaan tsygootti (Zy), joka kehittyy ookysta (Oo). Kypsymättömiä ookystien johdetaan ulosteet ja kypsyminen tarttuva sporuloineella ookystista tapahtuu ympäristössä. Tunnistettavissa vaiheissa tämän kypsymisen (eli sporogonia) sisältävät ookystien yhdellä sporoblast, ookystien kaksi sporoblasts, ja kypsä ookystien kaksi sporocysts, joista kukin sisältää neljä sporotsoiitteja. [Katso myös yksityiskohtainen keskustelu Cryptosporidium elinkaaren].
Oireet ja Patogeneesi. Oireita I Belli infektio ovat ripuli, steatorrhea, päänsärky, kuume, vatsakipu, pahoinvointi, nestehukka ja laihtuminen. Veri on harvoin läsnä ulosteissa. Yleensä oireet ovat samanlaisia kuin kryptosporidoosia. Tauti on usein itsestään. Se voi kuitenkin tulla krooninen kanssa ookystien havaitaan ulosteissa kuukausia tai vuosia ja recrudescences oireita. Tauti on yleensä vakavampia imeväisten ja pikkulasten kuin aikuisilla. Liittyvä patologia I belli infektiot ovat pääasiassa villusatrofian, tai blunting, ja kryptahyperplasian kuten tavallisesti nähdään muissa suoliston infektioita.
Ripuli AIDS-potilaiden on usein hyvin vetinen ja voi aiheuttaa kuivumista vaativat sairaalahoitoa. Kuume ja laihtuminen ovat myös yleinen löydös. Toinen yleinen löydös keskuudessa AIDS-potilailla on krooninen ajoittainen ripuli kestää kuukausia tai vuosia. Tuloksena oleva liiallinen laihtuminen ja elektrolyyttitasapainon häiriöitä voi johtaa tuhlaaminen ja jopa kuoleman. On ollut myös muutamia raportteja levitetään suoliston isosporiasis AIDS-potilailla.
Lindsay, DS, Dubey, JP, Blagburn, BL (1997) Biology of Isospora spp. ihmisistä, kädelliset ei-ihmiset ja kotieläimet. Clin. Microbiol. Ilm 10: 19-34.
Cyclospora
Ensimmäinen ihmisen tapauksessa Cyclospora cayetanensis ilmoitettiin vuonna 1979. Se oli alun perin nimitystä syanobakteerien kaltaisten elinten tai kokkidi kaltaisten elinten (CLB). Organismi vahvistettiin olevan kokkidi loinen, jossa on ookysta rakenne on samanlainen suvun Cyclospora ja sitten nimetty 1994 jälkeen Universidad Peruana Cayetano Heredia Perussa, jossa suurin osa aiemmissa tutkimuksissa oli tehty. Molecular tutkimukset osoittavat läheinen suhde Eimeria tärkeä eläinlääkärin loinen siipikarjan ja muiden eläinten. C. cayetanenis on maailmanlaajuinen jakelu, mutta se näyttää olevan erityisen suuri Latinalaisessa Amerikassa, Intian niemimaalle, ja Kaakkois-Aasiassa. Kehittyneissä maissa infektioita yleensä liittyy joko ruokamyrkytysepidemioihin tai turistiripulissa.
Elinkaari ja siirto. Elinkaaren Cylcospora on samanlainen Isospora (katso edellä). Infektio on hankittu nauttimisen kautta ookystien. Sprorozoites vapautetaan ja infektoivat epiteelisoluja ja ohutsuolen yläosassa. Loinen läpi merogony ja merotsoiitteja reinfect enterosyyttien ja useita kierroksia merogony voi esiintyä. Jotkut merotsoiittisukupolven tehdään seksuaalisen kehityksen tuloksena syntyy mikro- ja macrogametes. Hedelmöityksen macrogamete että microgamete aloittaa sporogonia ja muodostumista ookystien. Kuten Isospora Itiöintiä valmistunut ympäristöön ja kehittymätön tarttumaton ookystien erittyy ulosteisiin. Kypsymisen ookystojen sporuloineella tarttuvan ookystoja todennäköisesti kestää päivistä viikkoihin. Lisäksi rakenne Cyclospora ookystien on erilainen kuin Isospora. Ookysta sisältää kaksi sporocysts, jotka kukin sisältävät kaksi sporotsoiitteja.
Useita epidemioita Yhdysvalloissa ja Kanadassa on liittynyt tuoretuotteiden tuotu Etelä- ja Keski-Amerikka (taulukko). Erityisesti marjat ja lehtivihannekset on todettu todennäköinen saastunut tuote. Nämä ovat elintarvikkeita, jotka ovat tyypillisesti syödään raakana ja vain huuhdellaan. Ei tautitapauksia on yhdistetty jäädytetty, jalostettu tai kuorittuja hedelmiä tai vihanneksia. Kausiluonteisuudesta että epidemioiden on myös havaittu useimmissa tapauksissa esiintyy keväällä ja alkukesästä. Samanlainen kausiluonteisuus on havaittu endeemisiä myös. Toisin kuin Yhdysvalloissa ja Kanadassa, jossa elintarvikeperäisten lähetys hallitsee, suurin osa tapauksista Euroopassa ja Australiassa on matkustamiseen liittyvistä endeemisiä.
Valitut Cyclosporiasis tautitapauksia Yhdysvalloissa ja Kanadassa |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Modifioitu Herwaldt (2000), jotka päivitetään. Kysymysmerkkejä (?) Osoittamaan todennäköinen ajoneuvo tai lähteestä, mutta ei vahvistettu. |
Seurauksena suuri määrä tautitapausten liittyy vadelmia Guatemalasta Yhdysvalloista rajoitettu tuonnin vadelmat ja vaadittu tarkastus tiloilla. Tämä johti myöhemmin laskuun tautitapausten Yhdysvalloissa. Kanada, jotka eivät rajoita tuonnista, ei kokenut pisara tautitapausten tänä aikana. Myöhemmässä asiassa kontrolloituja tutkimuksia suoritetaan Guatemalassa paljasti, että infektiot olivat yleisimpiä lapsilla yleisyydessä korkeimmillaan kesäkuussa. Merkittävimmät riskitekijä liittyy infektioon joi käsittelemättömän veden. Perussa kosketusta maaperään tunnistettiin toinen riskitekijä, erityisesti lasten alle kaksi vuotias. Riittämätön veden käsittely näissä endeeminen maissa voi johtaa maan saastuminen veden ja siten ylläpitää lähetyksen aikana. Oletettavasti elintarvikeperäisiä siirto johtuu kastelu tai soveltamalla lannoitetta saastuneen veden tai pesu ja käsittely elintarvikkeita huonosti käsiteltyä vettä.
Oireet. Cyclospora ensisijaisesti infektoi epiteelisolujen yläosaan ohutsuolessa. Itämisaika on Yleensä kahdenkeskistä kaksi viikkoa. Oireet ovat samankaltaisia kuin suolistotulehdus aiheuttama Isospora ja Cryptosporidium joka tyypillisesti sisältää sykliä ripuli ja jaksojen ilmeinen remission. Ripuli on tunnusomaista usein ulosteet ja voi kestää jopa kuusi viikkoa, mutta on yleensä itsestään in immunocompent henkilöä.Ruokahaluttomuus, huonovointisuus, pahoinvointi ja kouristelua muitakin yleisiä oireita cyclosporiasis. Joissakin tapauksissa potilaille saattaa tulla oksentelua, lihassäryt, merkittäviä laihtuminen, ja räjähtävä ripuli. Edellinen altistuminen Cyclospora näyttää joskus antaa vastustuskykyä infektioita, joiden oireiden vähenemistä. Ajan aikuiset näyttävät vastustuskyvyn kehittäminen ja oireettomia kantajia löytyy endeemisillä alueilla.
Kuten asianlaita myös Cryptosporidium ja Isospora, ripuli aiheuttama Cyclospora AIDS-potilaiden on huomattavasti ankarampi kuin immunokompetenteille henkilöitä. Ripuli voi kestää kuukausia ja tuottaa oireyhtymä, joka on heikentäviä ja hengenvaarallisia.
Cyclospora arvostelut:
Sterling ja Ortega (1999) Clycospora: arvoitus arvoinen purkautumista. Emerging. Inf. Dis. 05:48.
BL Herwaldt (2000) Cyclospora cayetanensis: Katsaus keskitytään puhkeamisen clyclosporiasis 1990-luvulla. Clin. Inf.Dis. 31: 1040.
JM Shields ja BH Olson (2003) Cyclospora cayetanensis: katsaus syntymässä lois kokkidi. International Journal for Parasitology 33, 371-391.
LS Mansfield ja AA Gajadhar (2004) Cyclospora cayetanensis , elintarviketuotantoon ja vesiliikenne kokkidi loinen. Eläinlääkärin parasitologia 126: 73-90.
YR Ortega ja R Sanchez (2010) Cyclospora cayetanensis, elintarvikkeista aiheutuvan ja vesiliikenne loinen. Clin. Microbiol.Ilm 23: 218-234.
Diagnoosi ja hoito Suolen Coccidia
Kokkidioosin diagnosoitu osoittamalla ookystien ulosteet.Haponkestävien värjäys on edullinen menetelmä kokkidien, jotka tahra kirkkaan punainen. Cryptosporidium, Cyclospora, ja Isospora on tunnusomaista koko ja ookystien rakenne (taulukko). Cyclospora ja Isospora eivät tasaisesti vievät tahra jolloin saadaan seos, värjäämättömän, osittain värjätään ja täysin värjätään ookystien. Cyclospora ja Isospora voidaan myös havaita kautta autofluoresenssi liittyy kysta seinään.Koska sillä on suhteellisen suuri koko, Isospora on helposti havaittavissa värjäämättä yksilöitä. Sarcocystis on harvinainen ihmisen infektio (katso jäljempänä), jossa ookystoja samanlainen Isospora paitsi että sporocysts yleensä vapautuu ookystien silti suolistossa.
| Kokkidi Loiset Löytyy Human Ulosteet | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
Suositeltu hoito Cyclospora ja Isospora on yhdistelmä trimetopriimi-sulfametoksatsolin (Bactrim). Ei ole täysin tyydyttävää hoitoa Cryptosporidium. On arveltu, että ‘ekstrasytoplasminen’ sijainnin Cryptosporidium suojien sen huumeista. Paromomysiini on käytetty hoitoon kryptosporidoosia, mutta sen tehokkuus on keskusteltu. Hallittu tutkimukset osoittavat, että paromomysiinistä käyttämällä lähtöaineena vaatimattomasti vaimentaa-parasitemian immunokompromettoiduilla yksilöitä. Vaikeiden kryptosporidioosin tulisi sisältyä tukihoitoa (nesteytys ja ravitsemuksellinen tuki) ja anti-liikkuvuutta aineita. Ehkäisevät toimenpiteet on samanlainen kuin muut sairaudet lähettämän ulosteiden-suun kautta (ks riskitekijöitä tai Giardia kontrolli).
Kudoskystia Muotoilu Coccidia
Jotkut kokkidi lajit ilmentävät heteroxenous elinkaaren jossa merogony tapahtuu kudoksissa väli-isäntä (saalista) ja gametogony tapahtuu suoliepiteeliin lopullisten isännän (saalistaja). [Tavallisesti suvullisen lisääntymisen tapahtuu pääisännissä.] Suhteen ihmisen infektioiden, Toxoplasma on yhteinen kudos kysta muodostamiseksi kokkidi loinen, kun taas infektiot Sarcocystis lajit ovat melko harvinaisia.
Elinkaaren (katso kuvio) ja Sarcocystis sisällä Saalistajan (eli lihansyöjä) on samanlainen kuin elinkaaren suoliston kokkidien, kuten Isospora, johon kuuluu seksuaalinen sykli (gametogony) sisällä suolen epiteelisoluihin. Yksi ero Sarcocystis elinkaaren on puute merogony suolen epiteelisolujen. Toisin sanoen merotsoiitteihin hankittu syömällä tartunnan saalista tuottaa vain sukusoluja miehityksen jälkeen suolen epiteelisolujen. Fuusio sukusolujen johtaa tuotannon ookystien. Lisäksi sporocysts yleensä vapautetaan ookystien suolistossa vastaanottavan ja sen vuoksi tarttuva sporocysts löytyy ulosteet.
Väli-isäntien (herbivore) hankkivat tartunnan syömällä itiöitä sporocysts. Itiöiden kanssa vapautetaan, tunkeutuvat suolen epiteelisolujen, ja tehdään merogony mikä on tyypillistä suoliston kokkidien. Toisin kuin suoliston kokkidien, me- rotsoiitit hyökkää endoteelisolujen ja tuottaa systeeminen infektio. Varsin usein on tropismista tiettyjä kudoksia, kuten aivoissa tai lihasten. Meronts (tai skitsonttien) näissä kudoksissa ovat usein usein kapseloidaan ja nimitystä ‘kudoskystia’. Näiden kudoskystia, tai sarcocysts tapauksessa lihaksen, esiintyy usein alhaisempi replikaation aikana merogony ja ovat hieman lepotilassa. Nieleminen tartunnan saaneen eläimen lihansyöjä vapauttaa merotsoiitteihin joka tunkeutuu suoliston epitheial soluihin ja täten täydentää elinkaaren.
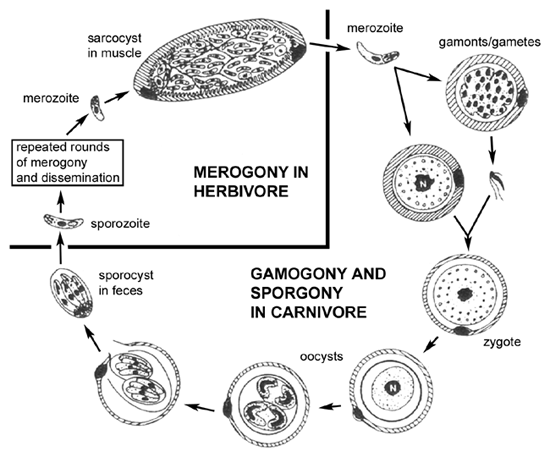
Tämä peto-saalis elinkaari ei ollut laadittu 1970-luvulle saakka. Aiemmin suolen infektioiden Saalistajan olivat yleensä nimetty Isospora lajien ja kudoksen infektioita saalis oli yleensä nimettiin Sarcocystis lajeja. Monissa tapauksissa pääisännissä ei varmuudella todettu ja taksonomian monien Sarcocystis laji on epävarmaa.
Sarcocystis ihmisille infektioita on dokumentoitu, mutta ne ovat harvinaisia. Ihmiset ovat lopulliset isäntä S. hominis (alias, S. bovihominis) ja S. suihominis määritettynä tartunnan lähde on joko naudan tai porsaan, vastaavasti. Nauttimisesta alikypsennetty naudan- tai sianlihaa tartunnan saaneista eläimistä tulee tuottaa suolistoinfektiota jotka voivat tuottaa akuutteja suolikanavan oireet (vatsavaivoja, pahoinvointia, ripulia). Kuitenkin useimmat infektiot uskotaan olevan oireettomia. Tartunnan saaneet ihmiset voivat irtoa sporocysts ulosteissa viikoista kuukausiin infektion jälkeen. Sporocysts ihmisen ulostetta ovat tartunnan lehmiä, sikoja ja poroja.
Ihminen voi myös toimia välituotteena isäntä ainakin joitakin Sarcocystis lajeja esiintyy luonnossa. Nieleminen sporocysts ihmisten voi johtaa kudoksen vaiheessa infektio ja muodostumista sarcocysts. Nämä sarcocysts ovat generaly useita 100 um ja aiheuttaa vähän kudosvaurioita. Kliinisiä oireita voivat olla lihasten arkuus tai ajoittainen tuskallinen tulehduksellinen turpoamista. Nämä lihakset kystat ihmisellä on ainoastaan satunnaisia ilmoituksia (<100 raportoitu tapauksia) ja edustavat luultavasti vahingossa infektioita. Yksi tutkimus totesi, että sarcocysts ihmisillä yleensä muistuttavat Sarcocystis lajeille, joita esiintyy paikallisessa apinoilla (Beaver et ai, Am. J. Trop. Med. Hyg. 28: 819, 1979). Suurin osa tapauksista on raportoitu trooppisilla ja subtrooppisilla Aasiassa, mukaan lukien puhkeaminen lihasten sarcocystosis suuressa suosiossa palaavat Malesiasta (MMWR 61:37).
Fayer, R (2004) Sarcocystis spp. Human infektioita. Clin.Microbiol. Ilm 17: 894-902.
Toksoplasmoosi
Toxoplasma gondii on kokkidi loinen, joka tarttuu ihmisiin sekä erilaisia nisäkkäitä ja lintuja. Se osoittaa saalistaja-saalis tyyppi elinkaaren (kuten edellä on Sarcocystis) ja kissat ovat vain lopullinen isäntä. Toksoplasmoosi esiintyy kaikkialla maailmassa (paitsi erittäin kylmissä tai kuivassa ilmastossa) ja yleensä se on yleisempää trooppisessa ilmastossa. Serologiset tutkimukset ovat osoittaneet esiintyvyys on jopa 70%, jonka ikä on 25 eräissä Keski-Amerikan populaatioiden. Yhdysvalloissa arviolta 0,5-1% väestöstä tulehtuu vuosittain yleisyys vaihtelee 10-25%: n 25-vuotiaita Toksoplasmoosi on useimmiten hyvänlaatuinen tauti. Totesi poikkeukset ovat tapauksia synnynnäinen infektio tai immuunivaste yksilöiden.
- Elinkaari
- Kliiniset ominaisuudet
- Diagnoosi, hoito ja ehkäisy
Elinkaari
Toxoplasma on monimutkainen elinkaari, joka koostuu suoliston ja kudoksen vaiheissa. Vaikka organismi havaittiin ensimmäisen kerran vuonna 1908, kuten kudoksessa loinen Gondi (an Afrikkalainen jyrsijä), sen koko elinkaaren ei ollut määritetty vasta vuonna 1970. suoliston vaihe infektio esiintyy vain kissa- ja sillä on tyypillinen suoliston kokkidi elinkaari, joka koostuu of merogony ja gamogony (ks Isospora elinkaari). Kissat saavat tartunnan syömällä eläimet tartunnan kudoksen vaiheen loisen. Loiset tunkeutuvat suolen epiteelisolujen ja tehdään merogony. Tuloksena merotsoiitit voidaan sitten joko tehtävä lisäkierroksia merogony tai tehdään gametogony. Kuten on samanlainen kuin muut Apicomplexa (katso yleinen Apicomplexan elinkaari) Makro- ja microgametes tuotetaan. Siten kissa pidetään pääisäntä koska tämä on isäntä, jossa seksuaalinen sykli tapahtuu.
Bi-flagelloitu- microgametes vapautuu suolen onteloon ja hedelmöittää macrogametes isännän epiteelisoluihin. Eritys ookystien seinän alkaa pian hedelmöityksen jälkeen. Tämä hormonikierron huipentuu tuotannossa ookystien joita poistuu ulosteen mukana. Nämä epäkypsä ookystien tehtävä sporogonia ympäristön lämpötilassa johtaa kypsän ookystien sisältää kaksi sporocysts, joissa jokaisessa on neljä sporotsoiitteja. Itiöinti kestää yleensä 1-4 päivää ja ookystien edelleen tartunnan kuukausia tummennetut kosteassa maaperässä. On oletettu, että ei-hedelmöitetty macrogametes voi myös kyetä muodostamaan kypsä ookystien (Ferguson, Tr. Parasitol. 18: 351, 2002).
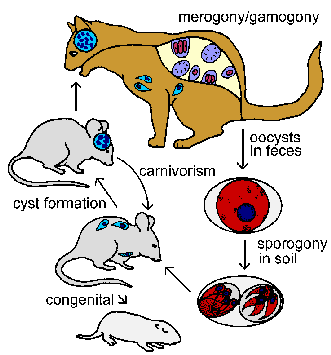 Väli-isäntiä, kuten jyrsijöiden ja lintujen, tartuttamia nauttimisen kautta sporuloineella ookystoja. Itiöiden kanssa vapautetaan, tunkeutuvat suoliepiteeliin, ja tunkeutua makrofagien ja muita soluja. Invaasio prosessi on tyypillistä Apicomplexa ja loisen sijoittuu parasitoforisten vakuolin. Sisällä vakuolissa loinen käy läpi binary fissio (eli merogony) ainutlaatuinen prosessi nimeltä endodyogeny. Endodyogeny on erikoistunut tyyppinen alue, jolla kaksi tytär solut muodostavat sisällä emosolun. Nämä trofia lomakkeet kutsutaan takytsoiittien (tachytarkoittaa nopea) viitaten niiden korkean replikaation. Isäntäsolun rikkoutumisen ja vapauttaa takytsoiitit, jotka tunkeutuvat uusia isäntäsoluja ja toista replikaatiosyklin. Tartunnan makrofagit levittää takytsoiitit koko isäntä aikana akuutti infektio.
Väli-isäntiä, kuten jyrsijöiden ja lintujen, tartuttamia nauttimisen kautta sporuloineella ookystoja. Itiöiden kanssa vapautetaan, tunkeutuvat suoliepiteeliin, ja tunkeutua makrofagien ja muita soluja. Invaasio prosessi on tyypillistä Apicomplexa ja loisen sijoittuu parasitoforisten vakuolin. Sisällä vakuolissa loinen käy läpi binary fissio (eli merogony) ainutlaatuinen prosessi nimeltä endodyogeny. Endodyogeny on erikoistunut tyyppinen alue, jolla kaksi tytär solut muodostavat sisällä emosolun. Nämä trofia lomakkeet kutsutaan takytsoiittien (tachytarkoittaa nopea) viitaten niiden korkean replikaation. Isäntäsolun rikkoutumisen ja vapauttaa takytsoiitit, jotka tunkeutuvat uusia isäntäsoluja ja toista replikaatiosyklin. Tartunnan makrofagit levittää takytsoiitit koko isäntä aikana akuutti infektio.
Koska isäntä kehittää immuniteetin replikaation hidastuu ja infektoituja isäntäsoluja tulee kapseloidun (eli kudoskystia). Näiden hitaasti replikoituvat muodot kutsutaan bradyzoites (Brady tarkoittaa hidas) ja ovat lepotilassa tai levossa vaiheessa. Bradyzoites pidetään metabolisesti lepotilassa, mutta jäävät eloon (Dubey ym, Clin. Microbiol. Rev. 11: 267, 1998). Muut muutokset, joita tapahtuu, kun takytsoiitteja muuntaa bradyzoites sisältää erityksen kitiinin ja muiden komponenttien muodostamiseksi kysta seinä ja kertymistä amylopektiinin rakeiden (mikä glukoosi varastointi). Kudoksen kystat Toxoplasma osoittavat eri kokoja, mutta usein saadaan koko on 50-70 um, jotka sisältävät 1000-2000 bradyzoites. Bradyzoites esiintyy pääasiallisesti aivoissa ja lihaskudoksen, kun taas takytsoiitit yleensä olla retikuloendoteliaalijärjestelmän soluissa.
Bradyzoite vaihe edustaa krooninen infektio ja todennäköisesti jatkuu elämän isäntä. Mekanismi tätä pysyvyys ei tunneta.Jotkut tutkijat uskovat kudoskystia ajoittain murtaa ja vapauttaa bradyzoites joka tunkeutuu uusia isäntäsoluja ja johtaa muodostumista enemmän kudoskystia.
Kudos vaihe infektio voi myös lähettää synnynnäisesti jälkeläisille ja muiden väli-isäntiä kautta carnivorism. Nauttiminen tartunnan saaneen eläimen vapauttaa bradyzoites kudoksesta kystat, joka sitten solujen infektoimiseksi uusi isäntä. Mahdollisesti kaikki nisäkkäät, mukaan lukien ihmiset, voivat saada tartunnan kanssa Toxoplasma. Kuten hankkia infektion nauttimisen kautta ookystien, loiset läpi akuutin vaiheen ominaista nopea replikaation seuraa kroonisen vaiheen tunnettu siitä, että lepotilassa kudoskystia. Nauttiminen tartunnan väli isännässä kissa aloittaa suolen vaiheessa elinkaaren johon merogony ja gamogony suolen epithial soluja. Kissat voivat myös tukea kudosta vaiheessa infektio.
| ihmiseen |
|---|
|
Ilmeisesti ihmiset eivät ole luonnollinen osa peto-saalis elinkaaren ja ovat vahingossa isäntä, joka ei osallistu jatkoa lähetyksen aikana. Yksi tartunnan lähde on nauttimisen materiaalin saastunut itiöidyillä ookystista erittyy kissojen. Tämä merkitsee jonkin yhdistyksen kanssa kissat. Koska ookystat täytyy kypsyä ympäristöön ennen tulossa tarttuva, siirto sisältää piirteitä maaperän lähetyksen samanlainen Isospora ja Cyclospora. Esimerkiksi lapset indeksointi ja likaa syöminen iät uskotaan olevan suurempi riski infektion. Ookystien voidaan hankkia myös kautta puutarhanhoitotarkoituksiin tai pesemätön hedelmiä tai vihanneksia. Lisäksi muutama vettä tautitapaukset on dokumentoitu. Korkeat esiintyvyys toksoplasmoosi Etelä- ja Keski-Amerikassa uskotaan johtuvan korkea ympäristön saastumista kanssa ookystien. Ironista kyllä, joutuessaan koirien on enemmän riskitekijä tartuntariskille Toxoplasma kuin joutuessaan kissoille. Tämä johtuu todennäköisesti koirille etsimällä kissan ulosteet ja kontaminoitumasta ulosteet ja sitten siirtämällä itiöitä ookystista vaatteisiin ja kädet niiden omistajille. Mielenkiintoista, vesiohenteinen puhkeaminen liittyy pennut elävät päälle kunnallisen vesisäiliön Brasiliassa raportoitu (de Moura ym, 2006, Emerging. Inf. Dis. 12: 326).
Toksoplasmoosi voidaan hankkia myös nauttimisen kautta huonosti kypsennetyn lihan, joka sisältää kudoskystia tai takytsoiitteja. Oletettavasti karjan hankkia infektiota laiduntaminen alueilla saastuttamia kissan ulostetta. Kyky loisen siirtämisen väli-isäntiä voivat olla suhteellisen uusi evoluution mukauttaminen loinen, joka yhtyy kesyttäminen kissan ja laajentaminen maatalouden (katso laatikko). Itse asiassa useimmat tartunnat Yhdysvalloissa ja Euroopassa keskuudessa aikuiset todennäköisesti hankitaan kypsennettyä lihaa. Erityisen korkea seropositiivista rate Ranskassa (90%) johtuu todennäköisesti kulttuurinen mieltymys puoliraakoina tai raakaa lihaa. Lampaanliha ja sianlihan ovat yleisempiä lähteitä kuin naudanlihaa. On ollut myös muutamia Yksittäisiä raportteja on Toxoplasma kautta lähetetään takytsoiittien pastöroimattomissa vuohen maidosta.
Toxoplasma voidaan lähettää myös äidistä sikiöön, usein kohtalokkaita seurauksia (katso alla). Synnynnäinen lähetys voi tapahtua vain akuutti infektio (eli takytsoiitteja) hankittu pregancy. Äitien krooninen infektio hankittu ennen raskautta eivät ole riskiä lähettämiseksi Toxoplasma. Lähetys Toxoplasma seurauksena elinsiirrot on myös mahdollista. Kudoskystia kroonisesti tartunnan elimen luovuttajan voi aktivoida kun istutetaan saastuneet elimen vastaanottajan. Lisäksi immunosuppressiivinen terapia voi myös aktivoida piilevän tartunnan toteamiseksi vastaanottaja. Hankinta takytsoiittien peräisin akuutisti sairastuneen kautta verensiirto on myös mahdollista. Lähettäminen elinsiirron tai siirron nyt harvinaisia, mutta.
Viime aikoina lisänneet Toxoplasma?
Molecular analyysi Toxoplasma isolaattien (lähinnä Pohjois-Amerikasta ja Euroopasta) paljastavat rajoitetun geneettistä monimuotoisuutta. Suurin osa (> 94%) isolaateista klusterin kolmeen erilliseen klonaalinen suvusta nimetty tyypin I, tyypin II ja tyypin III. Nämä kolme klonaalisia suvusta liittyvät läheisesti toisiinsa ja ne koostuvat eri seoksia vain kaksi alleelien lokukset testattu.Kolmesta voi olla syntynyt geneettisen rekombinaation ilmenevät viime 10000 vuosi (1). Tämä olisi rinnakkainen laajentamiseen ihmisen maatalouden ja mukauttaminen kotikissa. Siten, muutokset ihmisen toiminnasta on voinut johtaa valinnan ja nopea eteneminen Toxoplasma. Lisäksi nämä klonaalinen tyypit kaikki omaavat kyvyn kautta lähetettävän suoraan suun kautta välillä väli-isäntiä, jotka voivat ei ole biologinen ominaisuus esi Toxoplasma tai muiden läheistä sukua olevien lajien, kuten Neosporan (katso alla). Tämä hankinta suullista tarttuvuuden yhdistettynä Eläinten kesyttäminen voisi edistää nopeaa, ja ennen kaikkea suvuton laajentaminen Toxoplasma.
Kolme Toxoplasma genotyyppiä osoittavat myös eroja virulenssin (2). Esimerkiksi, I-tyypin loiset ovat erittäin virulentti hiirissä. Samoin tyypin I suhteettoman liittyy vakavia epätyypillisiin silmän toksoplasmoosi immunokompetenteilla yksilöiden ja vakava synnynnäinen toksoplasmoosi. Onneksi kuitenkin tyypin II infektiot taipumus hallita, erityisesti Yhdysvalloissa on kuitenkin jonkin verran näyttöä siitä, että Toxoplasma esittelee enemmän monimuotoisuutta Etelä-Amerikassa. Parannukset tietämyksemme Toxoplasma populaatiobiologian voi ratkaista nämä kysymykset ja torjumaan paremmin ja hoitoon.
- Su et ai (2003) Viimeaikaiset laajennus Toxoplasma parantamalla suun lähetyksen. Science 299, 414.
- Boothroyd ja Grigg (2002) Väestö biologia Toxoplasma gondii ja sen merkitys ihmisen infektio: älä eri kannat aiheuttavat eri sairautta? As. Opin. Microbiol. 5 438.
Kliiniset ominaisuudet
Toksoplasmoosi aikuisilla ja lapsilla ohi vastasyntyneen vaihe on yleensä hyvänlaatuinen ja oireetonta. Hankinta infektion kautta joko ookystien tai kudoskystia johtaa akuutti infektio, jossa takytsoiitteja levitetään koko kehon kautta imusuonien ja hematogenously. Tämä akuutti vaihe kestää useita viikkoja immuniteetti kehittyy. Vasta-aine tuotanto vaatii 1-2 viikkoa ja soluvälitteisen immuniteetin tapahtuu 2-4 viikkoa infektion jälkeen. Sekä humoraalisia että immuniteetti ovat tärkeitä, mutta soluvaste näkyy kriittinen muuntaminen akuutti (ts takytsoiitteja) ja krooninen (eli bradyzoites) infektio. (Katso elinkaari selostus tachy- ja bradyzoites.) Erityisesti voimakas Th1-vasteen, tunnettu siitä, että proinflammatoristen sytokiinien, kuten interleukiini-12, interferoni-gamma, ja tuumorinekroositekijä-alfa liittyy Toxoplasma infektio.
Oireiden ilmenee, ne ovat yleensä lieviä ja tyypillisesti kuvattu mononukleoosina kaltaisia vilunväristykset, kuume, päänsärky, lihaskipu, väsymys ja turvonneet imusolmukkeet. Nämä oireet ovat itsestään rajoittuvia ja häviävät viikoista kuukausiin. Krooninen lympadenopathy ilman kuumetta edelleen tai toistuvia jopa vuosi on myös havaittu oireena toksoplasmoosi. Harvoin immunokompetentit henkilöt näytteille vakavia oireita ja akuutti infektio melkein aina etenee krooninen vaiheeseen. Tämä piilevä infektio todennäköisesti kestää elämän potilaan tuottamatta mitään progressiivinen sairaus.
| Toxoplasmic Encecphalitis |
|---|
|
Toksoplasmoosi on pitkään huomattava, koska opportunistinen infektio osalta latenttien infektioiden immunosuppression vuoksi liittyy elinsiirtojen ja tietyt syövän hoitomuotoja. 1980- toxoplasmic aivotulehdusta muodostunut yleinen komplikaatio liittyy aidsiin. Arviolta 25-50% AIDS kroonista toksoplasmoosi kehittyy aivotulehdusta. Aktivoituminen infektio tapahtuu tyypillisesti silloin, kun CD4-solujen pudota alle 100 solua per mikrolitra. Varhainen oireet toxoplasmic aivotulehdus voi olla päänsärky, kuume, uneliaisuus ja mielentilan muutoksia progressioehtoisen keskeiselle neurologisia puutoksia ja kouristuksia. Tauti on lähes aina, koska aktivoituminen on piilevä infektio (katso laatikko) ja sillä on taipumus rajoittua keskushermostoon. Toisin sanoen, kudoksen kystat murtuminen ja julkaissut bradyzoites ovat muuttumassa takytsoiittia. (Katso elinkaaren selostus tachy- ja bradyzoites) polttoväli leesiot johtuvat tuhoutuminen isännän solujen välittömässä läheisyydessä. Muut aktivoidun sairauden, erityisesti retinokoroidiitin, keuhkotulehdus, myokardiitti ja myosiitti, voi joskus esiintyä yhdessä immunosuppressioon.
Carlos S. Subauste, toksoplasmoosi ja aids.
Synnynnäinen toksoplasmoosi
Toxoplasma voidaan välittää myös synnynnäisesti (eli istukan) jos äiti hankkii infektion raskauden aikana. Synnynnäinen (eli transplasentaalinen) infektiot ovat todennäköisemmin oireenmukaista kuin synnytyksen jälkeiseen infektioita ja voivat olla erityisen vakavia (ks Tulokset laatikko). Joitakin keskeisiä piirteitä ovat:
- siirto mahdollista vain akuutin vaiheen (eli primaarinen infektio saa tapahtua raskauden aikana)
- voi tapahtua vain kerran
- yksi kolmasosa äitien seroconverting raskauden aikana välittää infektio sikiöön
- esiintyvyys välillä 1 1000 ja 1 per 10000 elävänä syntynyttä
- vakavuus vaihtelee iän sikiön (ankarampaa varhain raskauden)
- lähetys on useammin myöhemmin raskauden
- infektio voi johtaa: spontaani abortti, ennenaikainen synnytys tai täysiaikainen tai ilman etenevä sairaus
- Tyypillinen tauti ilmenemismuotoja ovat: retinokoroidiitin aivojensisäinen kalkkeutumista, hydrokefalia, pienipäisyys, psykomotorinen häiriöt, kehitysvammaisuus, sokeus ja muut visuaaliset vikoja
-
Synnynnäinen Infektio Tulokset
5-10% kuolema (abortin tai vielä syntymän) 8-10% vakavia aivo- tai silmävaurioita 10-13% kohtalainen-vakavia visuaalinen haitoista 58-72% oireeton syntyessään, kehittää retinokoroidiitin tai neurologisia oireita myöhemmin
Silmään toksoplasmoosi
Retinokoroidiitin, tulehdus verkkokalvon ja suonikalvon (paksu verisuonten alue takaosassa silmä), on toinen kliininen ilmentymä Toxoplasma infektio. Retinochoroiditiis voi johtua synnynnäisten tulehdusten tai akuutin tai aktivoida infektioita hankittu syntymän jälkeen. Alunperin silmäoireita olivat useammin liittynyt synnynnäisten tulehdusten tai myöhään osoitus johtuu aktivoituminen synnynnäinen infektio. Kuitenkin, silmän toksoplasmoosi on raportoitu yhä useammin yhdessä akuuteissa infektioissa. On ehdotettu, että eri genotyypit tuottavat eri virulenssin erityisesti suhteessa siihen ilmaus silmäsairaus. Kun kyseessä on synnynnäinen infektion retinokoroidiitin voi kehittyä viikoista vuosiin syntymän jälkeen. Noin kaksikymmentä prosenttia henkilöistä, joilla on synnynnäinen infektioita voi ilmetä retinokoroidiitin syntyessään ja nuoruudessa 82% näytteille oireita.
Vauriot ovat keskeisiä luonteeltaan ja yleensä itsestään. Niiden uskotaan olevan seurausta kysta repeämän verkkokalvon uudelleen tapauksissa tai takytsoiitteja akuuteissa tapauksissa. Solut verkkokalvon muistuttavat läheisesti keskushermostoon. Granulomatoottinen vauriot voivat myös olla läsnä suonikalvon. Vauriot ovat yleensä kahdenvälisiä synnynnäisten tulehdusten ja yksipuoliset jos hankittu syntymän jälkeen. Eläinkokeet tarjoavat todisteita siitä, että verkkokalvon kuolion liittyvä vaurio johtuu leviämisen loisia, kun taas yliherkkyys vasteet toxoplasmic antigeenit ovat vastuussa oheisiin tulehdus. Oireita voivat olla näön hämärtyminen tai muut näköaistin viat. Vision voi parantaa resoluutiota tulehduksen. Toistuminen tauti on havaittu, mutta taajuus ja siihen vaikuttavista tekijöistä uusiutumisen eivät ole selkeitä. Tauti on harvoin etenevä Immunokompetenttien yksilöitä, mutta voi arpi verkkokalvolle. Kuitenkin tauti voi olla kovaa AIDS-potilaiden ja edelleen edistystä.
- GN Holland (2003) Silmään toksoplasmoosi: maailmanlaajuinen uudelleenarvioinnin: osa I: epidemiologia ja sairauden kulun. American Journal of Ophthalmology 136, 973-988.
- GN Hollanti (2004) Silmään toksoplasmoosi: maailmanlaajuinen uudelleenarvioinnin: osa II: taudin ilmenemismuotoja ja hallintaan. American Journal of Ophthalmology 137, 1-17.
Diagnoosi, hoito ja ehkäisy
Toisin kuin useimmat muut alkueläininfektiot, diagnoosi on harvoin kautta havaitsemiseen tai talteenotto organismien, mutta nojaa vahvasti serologinen menettelyjä. Loiset voidaan havaita biopsoiduista yksilöiden, buffy coat-soluja, tai aivo-selkäydinnesteestä. Kuitenkin, havaitaan takytsoiitteja näistä aineista voi olla vaikeaa. Nämä yksilöt voivat myös käyttää istutettiin hiirten tai kudosviljelmän soluja tai analysoitiin PCR: llä. Tulokset voivat olla harhaanjohtavia kuitenkin, koska monet ihmiset ovat altistuneet Toxoplasma ja satama kudoskystia (bradyzoites). Näin ollen, serologinen testit ovat suositeltava osa diagnoosi.
Serologisia diagnoosi Toxoplasma on monimutkaista, koska esiintyvyys seropositiivinen yksilöitä. Korkeat vasta-ainetitterit itse eivät ole lopullisia todisteita akuutti infektio. Synnynnäisten tulehdusten ovat yhtä vaikea diagnosoida serologisesti koska äidin IgG läpäisee istukan ja jatkuu useita kuukausia. Näyttöä akuutti infektio on korkea IgM-tiitterit ja/tai merkittäviä lisäyksiä yhteensä vasta-ainetiitterit yhdessä oireita.Kuvantamismenetelmiä (CT, MRI) voi myös olla käyttökelpoinen diagnoosissa toxoplasmic enkefaliitti.
Hoidon merkintöjen ja kesto:
- Oireenmukaista potilaita tulee hoitaa, kunnes oireet ovat hävinneet ja on näyttöä hankittu immuniteetti.
- Retinokoroidiitin potilaita on täydentää kortikosteroidien tukahduttaa tulehdusta.
- Raskaana olevat naiset tulisi käsitellä Spiramysiini estää sikiön tartuntaa.
- Vastasyntyneet tulisi hoitaa 12 kuukauden välttää myöhemmin esiintymisten retinokoroidiitin.
- Immuunivajauspotilaat on käsiteltävä. Hoitoa tulee jatkaa varten 4-6 viikkoa lopettamisen jälkeen oireet, minkä jälkeen profylaksia niin kauan kuin immunosuppression kestää.
Suositeltu hoito on synergistinen yhdistelmä pyrimetamiinin ja sulfadiatsiini täydentää yhdessä foliinihapon kanssa (Leucovorin®).
| ennaltaehkäisy |
|---|
Raakaa lihaa
Kissa ulosteet
|
Ennuste akuutti toksoplasmoosi immunokompetenteilla aikuisilla on erinomainen. Akuutit infektiot sikiölle tai pikkulapsille voi seurata toistuvat iskujen retinokoroidiitin. Käsittely ei näytä harventaa näitä hyökkäyksiä. Jos aloitettu riittävän ajoissa, hoitoon immunosuppressiopotilaita johtaa yleensä parannuksia, mutta recrudescences ovat yleisiä.
Valvontatoimia toksoplasmoosi keskittyä välttää kaksi suurta tartuntalähteiden: raakaa lihaa ja saastuneen kissa ulostetta. Ennaltaehkäisevien toimien (laatikko) sisältää: välttää nieleminen itiöitä ookystista tai kudoksen kystat, tuhoaminen tartunnan muodoissa (esim., Lämmitys), ja estää infektion lemmikit. Ennaltaehkäisy on erityisen tärkeää raskauden aikana, jolloin seuraukset tartuntojen tiukimmat.
Katsauksia Toxoplasma :
- Luku Toxoplasma gondii JP Dubey
- Pingotuskehyksen et ai (2000) Int. J. Parasitol. 30, 1217
- D. Hill, JP Dubey (2002) Toxoplasma gondii: siirto, diagnostiikkaan ja ennaltaehkäisyyn. Kliinisen mikrobiologian ja Infection 8: 634-640.
- DE Hill, S Chirukandotha ja JP Dubey (2005) biologia ja epidemiologian Toxoplasma gondii ihmisellä ja eläimillä. Animal Health Research sta 6: 41-61.
- JG Montoya ja O Liesenfeld (2004) toksoplasmoosi. The Lancet 363: 1965-1976.
| Neospora caninum | ||
|---|---|---|
Neospora caninum on läheistä sukua Toxoplasma gondii ja sillä on lähes identtinen morfologian. Kuten Toxoplasma, Neospora tartuttaa monia kotieläimiä ja on merkittävä syy abortteja ja kuolleena syntymisen naudoilla maailmanlaajuisesti. Lopulliset isännät ovat koirat, joilla on neuromuskulaarinen sairaus. Ihmiset eivät ole isäntä. Koirat saada tartunnan nauttimisen jälkeen tartunnan kudosten väli-isäntiä. Itiöimättömistä oocyts irtoaa ulosteissa ja itiöitä ympäristöön. Väli-isäntiä hankkia tartunta nauttimisesta sporuloineella ookystoja. Toisin kuin Toxoplasma, Väli-isäntiä ei voi hankkia tartunta nauttimisesta kudoksen muotoja muista väli-isäntiä. Tartunta voidaan lähettää synnynnäisesti ja loinen on helposti ylläpidetään naudan ja koiran pystysuora siirto. Luonnonvaraisiin sykli johon valkohäntäpeura ja Coyotes on myös todettu (Rosypal ja Lindsay, Tr. Parasitol. 21, 349. 2005).
Punatauti |
| historiallinen huomautus |
|---|
| Vuonna 1893 Smith ja Kilborne kertoi, että punkit tranmit B. bigemina, syy Texas karjan kuumetta. Tämä oli ensimmäinen osoitus niveljalkaisten leviävä tauti ja todennäköisesti vaikutteita myöhemmin löytö muuta vektoria tarttuvat taudit, kuten keltakuume ja malaria. |
Punatauti on harvinainen zoonoottinen tartunta punkit. Etiologinen aineet, Babesia lajit, ovat veren infektoivia loisia monenlaisia luonnonvaraisten ja kotieläinten kaikkialla maailmassa. Babesia ja Theileria muodostavat ryhmä nimeltä piroplasms, viitaten erytrosyyttien sisäisen muotoja, jotka ovat päärynän muotoinen joillakin lajeilla. Piroplasms aiheuttavat valtavia menetyksiä karjan endeemisillä alueilla. Is On arveltu, että rutto egyptiläisten karjan kuvattu Raamatun Mooseksen kirjassa on voitu punaista vettä aiheuttama kuumetauti B. bovis.
Kaksi piroplasm suvut yleensä erottaa puute ennalta punasolujen syklin Babesia ja puute transovarial lähetyksen Theileria (ks elinkaari alla). Molekyyli- tiedot osoittavat, että Babesia ja Theileria lajit eivät muodostavat vastaavat monophylogenic ryhmiä. Erityisesti monet Babesia lajeja, jotka oli epävirallisesti ryhmitelty ‘pieniä’ Babesia, ovat läheisempää sukua Teileria. Yhdenmukaisesti tämän molekyylisulan tiedot, yksikään pieni Babesia-toisin kuin ‘suuri’ Babesia-hän lähetettävän transovarially puutiaisissa, mikä osoittaa tarvetta joidenkin uudelleenarviointia piroplasm luokituksen. (Katso G Uilenberg, 2006, Babesia-historiallinen katsaus, Veterinary parasitologia 138, 3-10.)
| ihmisen babesioosi | ||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
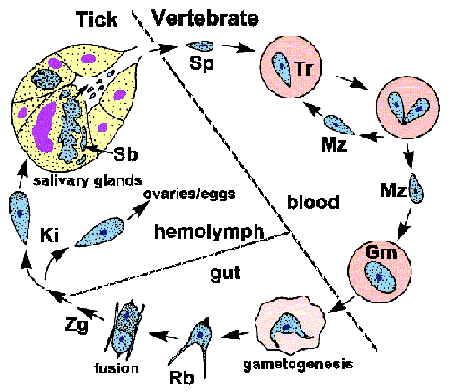
* Peurahiiret leucopus (valkojalkainen hiiri) ja Microtus pennsylvannicus vastaavasti. Monet lajit Babesia on raportoitu tarttua ihmiseen. Kolme eniten vallitseva laji tartuttamaan ihmiset ovat B. microti, B. duncani, ja B. divergens (taulukko). Infektiot muut lajit ovat joko huonosti dokumentoituja tai rajoittuu muutamiin yksittäisiin tapauksiin. Alkuperäisen tapaukset liittyvät pernan tai muiden immuniteettia vaarantamatta olosuhteissa. Kuitenkin immunologiseen pätevien henkilöiden tartunnan Babesia ja jossa ei ole kliinisiä oireita on kuvattu. Lisäksi serologisten tutkimusten mukaan tartunta voi alle diagnosoitu. Suurin painopiste ihmisten infektioiden Yhdysvalloissa on ollut pitkin Koillis kylki alueella, jonka perusteella nimi Nantucket kuume, ja ylempi keskilännen. Infektio Euroopassa on ilmeisesti harvinaisempaa sitten Yhdysvalloissa, mutta kohtalokas. Useimmat näistä infektioista on liittynyt henkilöitä, jotka ovat usein yhteydessä karjaa. ElinkaariBabesia osoittaa tyypillinen Apicomplexan elinkaari tunnettu siitä merogony, gametogony, ja sporogonia (kuvio). Infektio on hankittu selkärankaisen isännän, kun sporotsoiitteja (Sp) siirretään aikana rasti ruokinta. Itiöt hyökätä punasolujen käyttäen mekanismi hyökkäyksen, joka on samanlainen kuin muut Apicomplexa. (Katso yksityiskohtainen keskustelu isäntäsolun invaasiota malarialoisiosta). Toisin kuin Plasmodium parasitoforisten vakuolaarinen kalvo (PVM) hajoaa invaasion jälkeen ja loinen on suorassa kosketuksessa vastaanottavan erytrosyyttien sytoplasmaan. Trophozoites (Tr) jaa binaarinen fission ja tuottaa merotsoiitteihin (Mz), joka infektoitiin lisäksi erytrosyytit ja aloittaa uudelleen replikaatiosyklin. Joillakin lajeilla, tetrad, kutsutaan Maltan risti, on joskus havaittu.
Jotkut trophozoites kehittyy gametosyyttien (GM), tai gamonts, jotka ovat vastuussa aloittamisen infektion punkkikantajan.Gametosyyttien tehdään morfologisia muutoksia punkin suolistossa ja kehittyä ray elinten (R b; alias Strahlenkörper).Kaksi ray elinten (eli sukusolut) sulautuvat muodostaen tsygootti (ZG), joka sitten kehittyy kinete (Ki). Kinete tunkeutuu peritrophic kalvon ja suoliston epiteelin päästä hemolymfassa.Suuri Babesia, tällainen B. divergens ja B. canis, pystyvät tunkeutumaan eri elinten ja jatketaan edelleen replikaation.Merkittävin on hyökkäys munasarjat ja munia johtaa transovarial lähetyksen punkin jälkeläisiä. Sporogonia aloitetaan, kun kinetes hyökätä sylkirauhasten.Loinen laajenee ja täyttää ylipaisunut isäntäsolun ja kehittyy monitumaisia sporoblast (Sb, eli sporont). Mature sporotsoiitilla, jolla apikaalisella soluelimiin, se alkuunsa tästä eriytymättömiä sporoblast kun punkki jälleen uuden isännän. Viiden kymmenentuhatta sporotsoiiteista voidaan tuottaa yhdellä sporoblast. Itiöt on sitten injektoida isäntäorganismiin syljen kanssa, mikä täydentää elinkaaren.
|

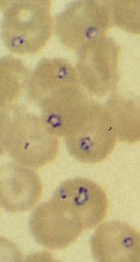 Diagnoosi on varmistettu ilmaisemalla loinen Giemsa-värjättiin verinäytteet. On mahdollista Babesia on sekoitettavissa malaria loinen, koska joitakin morfologisia yhtäläisyyksiä Plasmodium rengas-vaiheessa loisia (katso kuvio of B. microti). Serologia ei saatu vastauksia malarialääkkeet, eikä matkustushistoria muita tekijöitä harkitsemaan tekemään diagnoosin.
Diagnoosi on varmistettu ilmaisemalla loinen Giemsa-värjättiin verinäytteet. On mahdollista Babesia on sekoitettavissa malaria loinen, koska joitakin morfologisia yhtäläisyyksiä Plasmodium rengas-vaiheessa loisia (katso kuvio of B. microti). Serologia ei saatu vastauksia malarialääkkeet, eikä matkustushistoria muita tekijöitä harkitsemaan tekemään diagnoosin.